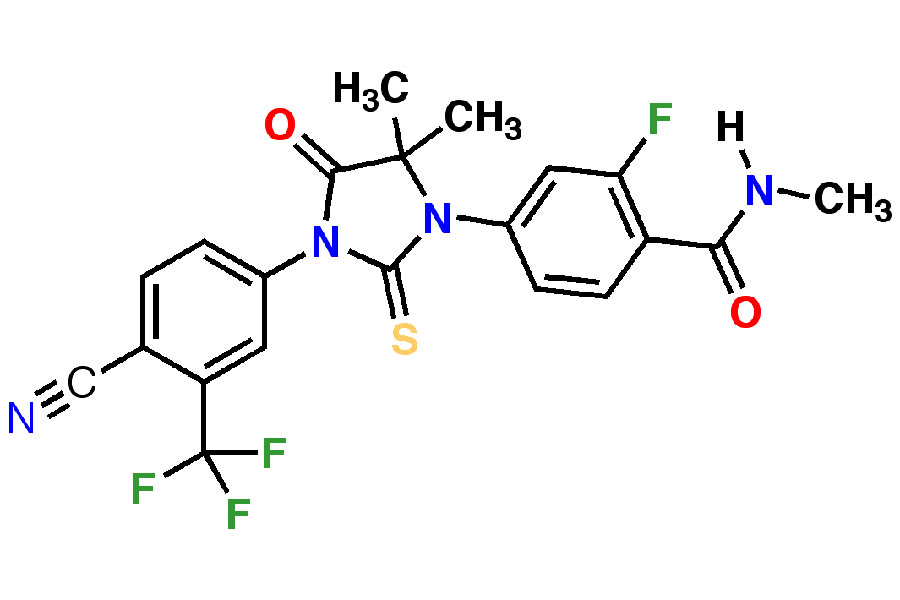
Рак предстательной железы (РПЖ) сейчас является одним из наиболее часто встречающихся злокачественных новообразований у населения мужского пола. В перечне онкологической заболеваемости в России среди мужчин РПЖ занимает второе место после рака легкого и третье место в списке смертности. РПЖ у лиц моложе 40 лет наблюдается редко, в среднем возраст заболевших 50-70 лет. За последние 10 лет возможности медикаментозного лечения пациентов с метастатическим РПЖ (мРПЖ) очень увеличились. Несмотря на то, что андроген-депривационная терапия (АДТ) по-прежнему является главным вариантом лечения, добавление цитотоксических и гормональных препаратов нового поколения улучшает онкологические результаты лечения пациентов с метастатическим гормоночувствительным (мГЧРПЖ) и кастрационнорефрактерным РПЖ (КРРПЖ). По результатам двух крупных рандомизированных исследований ARCHES и ENZAMET, препарат энзалутамид является стандартом лекарственной терапии не только при метастатическом и неметастатическом КРРПЖ, но и при мГЧРПЖ. Были привидены клинические наблюдения, которые показали высокую эффективность энзалутамида при различных формах рака предстательной железы. В первом клиническом случае, энзалутамид применялся при лечении метастатического гормоночувствительного РПЖ. Благодаря данной терапии пациент без признаков прогрессирования заболевания находился 11 месяцев. Во втором клиническом случае, энзалутамид применялся при лечении КРРПЖ, где также показал свою эффективность. Благодаря этому варианту лечения отмечены положительная динамика по уровню ПСА, стабилизация процесса по данным радиологического обследования. В данном случае, без признаков прогрессирования заболевания пациент находился 9 месяцев. На фоне этого варианта лечения отмечен более длительный контроль над болезнью по сравнению с предыдущими опциями лекарственной терапии.
Энзалутамид был открыт в Калифорнийском университете в Лос-Анджелесе, где идентифицировали энзалутамид и RD-162 как соединения свинца. Они были запатентованы в 2006 году и описаны в 2007 году. Энзалутамид был разработан и выпущен на рынок компанией Medivation для лечения рака предстательной железы. Затем был одобрен США (FDA) для лечения метастатического кастрационно-резистентного рака предстательной железы в августе 2012 года и для лечения неметастатического кастрационно-устойчивого рака предстательной железы в июле 2018 года. Энзалутамид был первым новым антагонистом AR, одобренным для лечения рака предстательной железы более чем за 15 лет, после введения НПВП первого поколения бикалутамид в 1995 году. Это был первый НПВП второго поколения, который был представлен.
Энзалутамид обладает примерно в 8 раз более высокой аффинностью связывания с рецептором андрогена (AR) по сравнению с бикалутамидом. По клиническими данным, энзалутамид - более мощный и эффективный антиандроген по сравнению с НПВП первого поколения, такими как бикалутамид, флутамид и нилутамид. Также не было доказательств гепатотоксичности или повышения уровня печеночных ферментов при лечении энзалутамидом.
В декабре 2019 года FDA одобрило применение энзалутамида для лечения людей с метастатическим раком предстательной железы, чувствительным к кастрации (mCSPC).
В июне 2023 года FDA одобрило талазопариб в комбинации с энзалутамидом для лечения людей с метастатическим кастрационно-устойчивым раком предстательной железы с мутацией в гене гомологичной рекомбинации (HRR) (mCRPC).
В ноябре 2023 года FDA одобрило энзалутамид для лечения людей с неметастатическим чувствительным к кастрации раком предстательной железы с биохимическим рецидивом с высоким риском метастазирования (BCR высокого риска).
Энзалутамид был открыт в Калифорнийском университете в Лос-Анджелесе, где идентифицировали энзалутамид и RD-162 как соединения свинца. Они были запатентованы в 2006 году и описаны в 2007 году. Энзалутамид был разработан и выпущен на рынок компанией Medivation для лечения рака предстательной железы. Затем был одобрен США (FDA) для лечения метастатического кастрационно-резистентного рака предстательной железы в августе 2012 года и для лечения неметастатического кастрационно-устойчивого рака предстательной железы в июле 2018 года. Энзалутамид был первым новым антагонистом AR, одобренным для лечения рака предстательной железы более чем за 15 лет, после введения НПВП первого поколения бикалутамид в 1995 году. Это был первый НПВП второго поколения, который был представлен.
Энзалутамид обладает примерно в 8 раз более высокой аффинностью связывания с рецептором андрогена (AR) по сравнению с бикалутамидом. По клиническими данным, энзалутамид - более мощный и эффективный антиандроген по сравнению с НПВП первого поколения, такими как бикалутамид, флутамид и нилутамид. Также не было доказательств гепатотоксичности или повышения уровня печеночных ферментов при лечении энзалутамидом.
В декабре 2019 года FDA одобрило применение энзалутамида для лечения людей с метастатическим раком предстательной железы, чувствительным к кастрации (mCSPC).
В июне 2023 года FDA одобрило талазопариб в комбинации с энзалутамидом для лечения людей с метастатическим кастрационно-устойчивым раком предстательной железы с мутацией в гене гомологичной рекомбинации (HRR) (mCRPC).
В ноябре 2023 года FDA одобрило энзалутамид для лечения людей с неметастатическим чувствительным к кастрации раком предстательной железы с биохимическим рецидивом с высоким риском метастазирования (BCR высокого риска).